Applications dans les laboratoires chapitre 1
Le principe de l’absorption de photons par la matière, basé sur l’effet photoélectrique, est largement utilisé pour caractériser cette matière dans les laboratoires, mais aussi dans le monde médical (radiographie, imagerie médicale) et dans le monde industriel (analyse chimique, radiographie,…). Sont présentés ici deux types d’appareillage largement utilisés aussi bien en physique qu’en chimie : la spectroscopie de photoémission et l’analyse de la matière par rayonnement synchrotron. La première technique conduit à des appareillages de taille modeste utilisables dans de « petits » laboratoires. La seconde technique nécessite un accélérateur de particules (électrons ou positrons) permettant de créer des faisceaux de rayons X extrêmement intenses sur une large gamme d’énergie (10eV à 100keV). Ce type d’appareillage est un laboratoire à lui seul qui fonctionne 24h sur 24 et qui fournit des photons pour une trentaine de postes expérimentaux (on parle de lignes de lumière), il permet de faire travailler simultanément un grand nombre de chercheurs dans des domaines aussi variés que la physique, la chimie, la biologie, la géologie, la médecine ou l’expertise historique ou/et artistique. Certaines lignes sont de plus ouvertes aux industriels pour des caractérisations spécifiques.
1 - La spectroscopie de photoélectrons excités par rayons X
Physique général
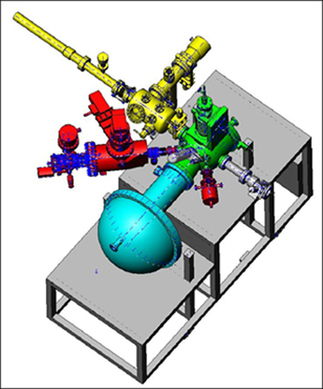
Le principe de ce type d'analyse est le suivant : on envoie un faisceau de rayons X sur l'échantillon et on détecte les électrons émis par effet photoélectrique. Cette technique permet ainsi de détecter les électrons provenant des différentes couches électroniques de l'atome excité, correspondant à des énergies bien précises qui varient d'un élément chimique à l'autre. Cette expérience se fait sous vide, puisque les électrons interagissent fortement avec la matière. Un exemple d’expérience de laboratoire est donné ci-dessous Cette technique est plus communément appelée XPS ou UPS, initiales de X-Ray Photoelectron Spectroscopy et Ultra-violet Photoelectron Spectroscopy.

Physique des processus d'excitation
Si le photon incident a une énergie suffisante pour amener l'électron d'un niveau de cœur vers le niveau du vide, l'électron pourra sortir de l'atome : c’est l’effet photoélectrique. Le schéma suivant va nous permettre de relier l'énergie du photon incident absorbé avec l'énergie de liaison de l'électron dans l'atome et l'énergie cinétique acquise par un électron éjecté hors de l’atome lors du processus d'absorption :
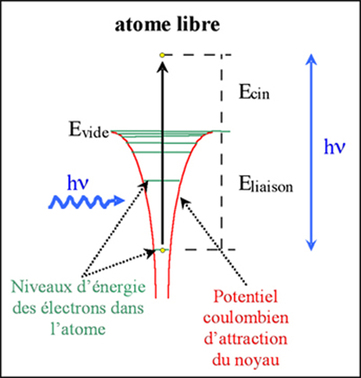
L’électron se trouve sur un des niveaux d’énergie autour du noyau. Il est attiré par le potentiel coulombien du noyau. Si on éloigne l’électron du noyau, il ne verra plus l’attraction en 1/r. Pour cela, il faut lui fournir de l’énergie. L’énergie du vide (ou d’ionisation) est définie comme l’énergie à fournir pour amener l’électron loin du noyau de telle manière qu’il soit « libéré », c'est-à-dire qu’il ne ressente plus cette attraction. Pour l’atome d’hydrogène, c’est précisément l’énergie de Rydberg, soit 13,6 eV. Si le photon incident possède une énergie au moins suffisante pour amener cet électron au niveau du vide, alors l’effet photoélectrique a lieu. S’il possède une énergie plus grande, l’excès d’énergie est alors acquise par l’électron sous forme d’énergie cinétique. Ainsi, dans un gaz, on a la relation suivante reliant l’énergie du photon, l’énergie de liaison de l’électron dans l’atome, et son énergie cinétique acquise :
Etant donné que les niveaux d’énergie des électrons dans l’atome sont discrets, on détectera ainsi des électrons ayant des énergies cinétiques bien précises, complètement corrélées à la structure électronique de l’atome excité. Notez que cette structure électronique change considérablement d’un élément chimique à l’autre : le potentiel du noyau augmentant à chaque fois qu’on rajoute un proton, les premiers niveaux d’énergie sont de plus en plus liés à mesure qu’on se déplace dans le tableau périodique, donc les énergies de liaison de plus en plus grandes. On remarque ainsi qu’une telle technique peut permettre d’identifier les éléments chimiques constituant le matériau analysé. C’est effectivement la fonction première de la spectroscopie de photoélectrons.
Analyse des spectres mesurés
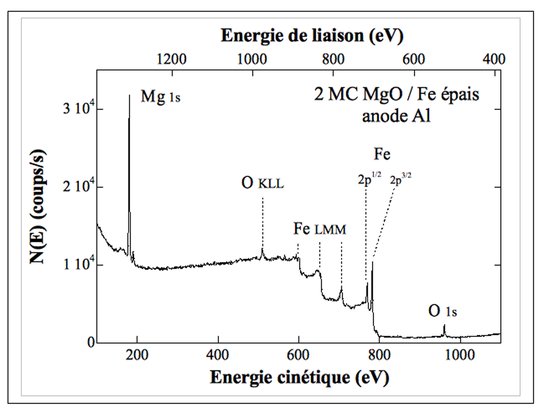
L'identification des pics obtenus est réalisée comme suit : on dispose de tables qui donnent les spectres XPS pour tous les éléments du tableau périodique (exceptés H et He qui donnent des intensités trop faibles). Les pics des spectres obtenus sont référencés par rapport aux niveaux d’énergie connus. Pour obtenir les énergies de liaison des éléments, ainsi que les rendements d’ionisation (on parle de sections efficaces) ou autres renseignements divers, de nombreux sites web sont disponibles (voir par exemple http://www.lasurface.com). Un exemple de spectre est donné sur la figure ci-après. Il a été obtenu sur une surface de fer recouverte de 2 plans atomiques de MgO, en utilisant le rayonnement X Kα de l’aluminium, obtenu en excitant les électrons de Al qui en redescendant sur un niveau plus lié émettent des photons X. L'énergie en abscisse est l'énergie cinétique, et nous avons également reporté l’énergie de liaison c’est à dire en calculant :
Le bilan des énergies n'est pas tout à fait le même pour un atome excité dans un gaz (atome libre) ou dans un solide (atome lié) où il faut vaincre le potentiel de sortie (attraction de tous les noyaux du cristal) mais ce point n’est pas primordial pour la compréhension. En examinant les tables donnant les niveaux d’énergie pour chaque élément pur, on identifie aisément le premier pic à faible énergie cinétique (donc forte énergie de liaison) comme provenant du premier niveau de Mg. Puis apparaissent les transitions de cœur du fer. Enfin, on observe le pic du premier niveau de l’oxygène. Nous verrons à la fin de ce cours les dénominations données à ces niveaux (1s, 2s, 2p….) :
2 - Analyse de la matière par Rayonnement Synchrotron
En photoémission, les appareils de laboratoire sont limités car la source de photons n’émet en général qu’à une ou deux énergies fixes. Il existe cependant des appareils qui permettent d’obtenir des photons X dans une grande gamme d’énergie, ou de longueur d’onde (on parle de rayonnement blanc). Un tel rayonnement blanc peut être obtenu en réalisant qu’une particule chargée peut émettre des photons lorsqu’elle subit une décélération. Il « suffit » ainsi d’accélérer par exemples des électrons (faciles à produire) à l’aide d’un accélérateur linéaire, puis de faire passer le faisceau dans un champ magnétique perpendiculaire à la vitesse des électrons. La trajectoire des électrons devient donc curviligne puisque les électrons subissent une accélération centripète due à la force de Lorentz .
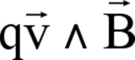
Cette accélération provoque l’émission de photon X si l’énergie des électrons est grande (la vitesse des électrons est alors proche de la vitesse de la lumière), comme le montre la figure suivante :
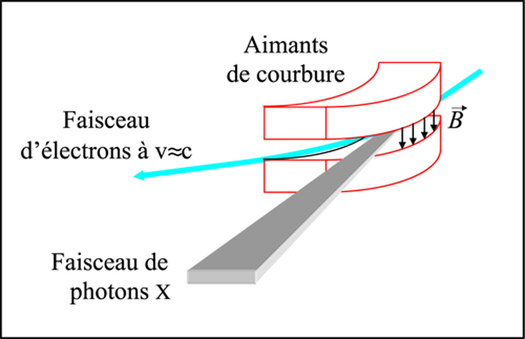
Des aimants dits de courbure sont utilisés. Il est ainsi possible de faire tourner le faisceau d’électrons dans un anneau refermé sur lui-même, permettant ainsi d’obtenir un faisceau de rayons X à chaque passage des électrons. Le rayonnement est émis dans une large bande d’énergie. Un schéma de principe est donné sur l’image suivante :

Il existe environ 70 synchrotrons dans le monde, dont 2 en France : le synchrotron européen ESRF situé à Grenoble construit en 1995, et le synchrotron français SOLEIL en service depuis 2007. Pour plus d’information voir le lien : www.journaldunet.com/video/9506/le-synchrotron-soleil/
Différents types d’expériences réalisables
Comme nous l’avons vu, les électrons du cortège électronique des atomes peuvent absorber des photons pour aller vers un niveau d’énergie plus élevé. Une fois sur un niveau élevé en énergie, ils peuvent être éjecté comme en photoémission si l’énergie du photon incident est suffisamment grande. Ils peuvent également redescendre sur un niveau plus lié du cortège électronique (diminuant ainsi l’énergie totale de l’atome), et dans ce cas émettre un photon. En raison de ces différents processus décrit par le modèle de Bohr, la réponse de la matière soumise à un tel rayonnement X peut être multiple :
- Diffraction ou diffusion du faisceau selon la structure de la matière
- Absorption -Transmission du faisceau après atténuation à travers la matière
- Photoémission
- Fluorescence : émission de photons par désexcitation
Un très grand nombre d'expériences sont donc possibles, d'autant que l'on peut choisir la longueur d'onde du rayonnement incident en utilisant des monochromateurs, et par exemple l'adapter exactement à l'écart d'énergie entre 2 niveaux du cortège électronique d'un élément : on obtient ainsi un phénomène de résonance. Il est également possible de choisir la polarisation des photons, linéaire ou circulaire, et d'étudier la réponse de la matière en fonction de cette polarisation. Les atouts d'une telle machine sont donc multiples. Tout d'abord, l'intensité du rayonnement obtenu est très importante, ce qui permet d'étudier des quantités infimes de matière. Le deuxième atout de taille est la sélectivité chimique, en gardant à l'esprit qu'il est possible de travailler à la résonance, et de jouer sur la polarisation. Enfin, pour les synchrotrons de dernière génération, des progrès importants ont été réalisé afin d'améliorer la résolution spatiale. Evidemment, la richesse des expériences réalisables intéresse les chercheurs de nombreuses branches des sciences dites dures comme la physique, la chimie, la biologie, la médecine mais aussi la géologie ou l'expertise artistique ou/et historique. Ce type d'appareillage est donc ouvert à toute la communauté scientifique. Pour obtenir du temps d'expérience, le chercheur doit écrire une proposition d'expérience examinée par des comités d'experts qui accordent ou non du temps en fonction de la demande et de la qualité du projet présenté. A titre indicatif, l'ESRF accueille environ 4000 chercheurs par an pour des durées d'expérience entre 1 jour à plusieurs semaines.
